世界口腔日 | VITA OralMicrobiome正式发布,助力实现口腔微生态单细菌功能解析
一、口腔菌群:从局部生态到全身健康
口腔是人体与外界环境直接接触的重要门户,也是人体仅次于肠道的第二大微生态系统。人类口腔中定殖着700 余种细菌、真菌及病毒,形成结构复杂且动态变化的口腔微生态。这些微生物参与牙菌斑形成、营养代谢及局部免疫调节,在维持口腔稳态中发挥重要作用。
当菌群结构发生失衡时,可直接驱动多种口腔疾病的发生。例如,变异链球菌(Streptococcus mutans)等产酸菌过度增殖会导致牙釉质脱矿并诱发龋齿;牙龈卟啉单胞菌(Porphyromonas gingivalis)等牙周致病菌则可破坏牙周组织,引发慢性炎症和骨吸收,最终导致牙周炎。
近年来的研究进一步发现,口腔菌群的影响并不限于局部组织。部分细菌可通过血液循环或吞咽进入远端器官,或通过诱导系统性炎症反应影响机体免疫稳态,从而参与多种全身疾病的发生发展。例如,牙龈卟啉单胞菌被认为与阿尔茨海默病和动脉粥样硬化相关,而具核梭杆菌(Fusobacterium nucleatum)则被发现能够在结直肠癌中富集并促进肿瘤进展[3]。
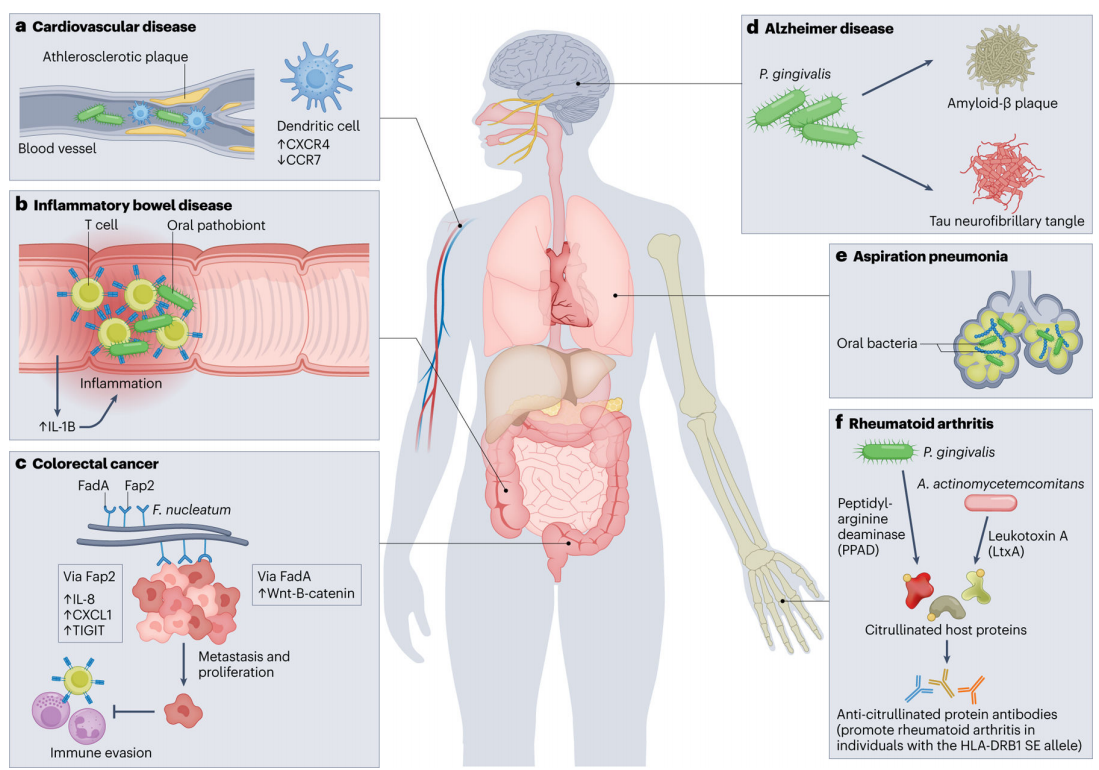
图1. 口腔菌群与全身系统疾病的关联[3]
二、传统宏组学在口腔菌群研究中的局限性
目前研究人员解析口腔菌群组成和功能主要依赖宏基因组与宏转录组。宏基因组可在 DNA 水平解析物种组成并预测潜在功能基因,但口腔菌群存在较高基因冗余[4],不同物种常携带相似功能基因,因此难以将具体功能归因到特定菌种。此外其反映的只是基因层面的“潜在能力”。宏转录组能够在 RNA 水平反映群体的基因表达和整体功能活性,但获得的仍是群体平均信号,容易掩盖关键活性亚群的真实表达特征。因此,传统宏组学方法往往难以识别真正驱动疾病或生态变化的关键功能物种或功能亚群,在阐释致病机制方面仍存在明显不足。
近年来,微生物单细胞转录组技术为解决这一问题提供了新的研究路径。该策略已在肠道菌群研究中得到验证,例如研究发现单形巨单胞菌(Megamonas funiformis)在不同宿主环境中可呈现截然不同的代谢功能状态[5],而这种功能差异在传统宏基因组或宏转录组的群体平均信号中往往难以被识别。
综上可见,要真正理解复杂菌群中的功能差异,仅依赖群体平均信号仍然不足,口腔菌群研究亟需引入微生物单细胞转录组检测技术。
三、VITA OralMicrobiome:推动口腔菌群研究迈入单细菌时代
今天,面对口腔菌群功能研究对单细菌分辨率技术日益增长的需求,M20 Genomics正式推出了面向口腔菌群的高通量单细菌转录组解决方案—— VITA OralMicrobiome,为研究者提供覆盖样本处理到数据分析的一站式研究工具。

图2. VITA OralMicrobiome产品图
VITA OralMicrobiome 采用随机引物策略,在单个细菌层面实现 RNA 的高效捕获与细菌标记,可对复杂口腔菌群中的数千至上万个细菌进行转录组解析。相比宏基因组和宏转录组获得的群体平均信号,该技术能够在单个细菌分辨率下识别不同物种及同一物种内部的功能差异,从而解析细菌的代谢状态、功能亚群及其潜在生态作用。
应用实测:单个细菌视角下的牙周炎机制解析
在近期发表于《Cell Host & Microbe》的一项研究[4]中,研究者利用 VITA OralMicrobiome 对 8 名健康受试者与 8 名牙周炎患者的口腔样本进行了检测分析。检测共捕获 133,458 个细胞,经严格质量控制后获得 10 万余个高质量的细菌,覆盖 57 个核心活跃物种,并基于高分辨率功能检测数据进一步解析牙周炎患者的龈下菌斑功能变化及致病机制。
01 揭示功能重构,而非简单物种替代
研究表明,健康与牙周炎状态下的菌群差异主要体现在功能状态的系统性重编程,而非物种组成的简单更替。在牙周炎患者中出现跨物种的表达趋势:口腔菌群整体下调与有氧能量代谢相关基因(如 TCA 循环),同时上调与发酵代谢相关基因(如乳酸脱氢酶 LdhA),提示在疾病状态下,龈下细菌的能量获取策略由氧化代谢转向发酵代谢(图3)。
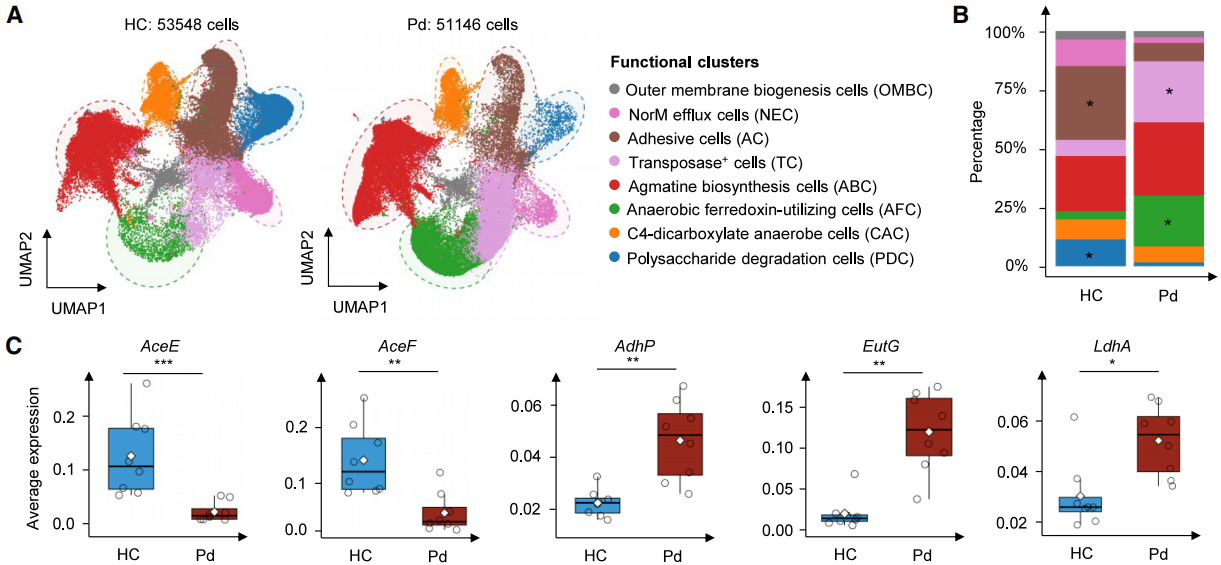
图3. 牙周炎状态下龈下菌群功能结构的重构[4]
此外,延长奈瑟菌(Neisseria elongata)在牙周炎患者中的分类丰度基本稳定(1.55% vs 1.36%),但其转录活跃细胞数量却由 4,334 个降至 870 个,负责黏附、Ⅵ型分泌系统及翻译调控的功能亚群比例明显减少(图4)。体外实验进一步表明,牙周炎相关的厌氧环境会抑制其转录活性,从而削弱其生态位竞争能力。该结果进一步支持:疾病相关差异主要体现在细菌的功能状态与活跃度变化,而非简单的物种更替。
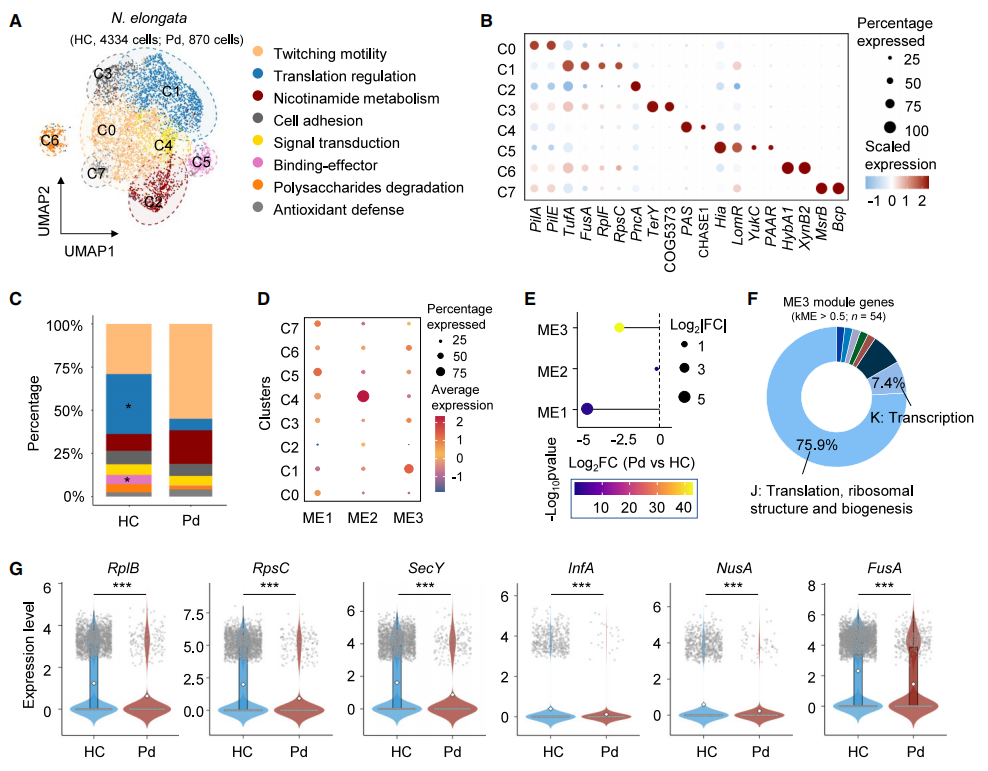
图4. 牙周炎状态中延长奈瑟菌的功能异质性及转录抑制[4]
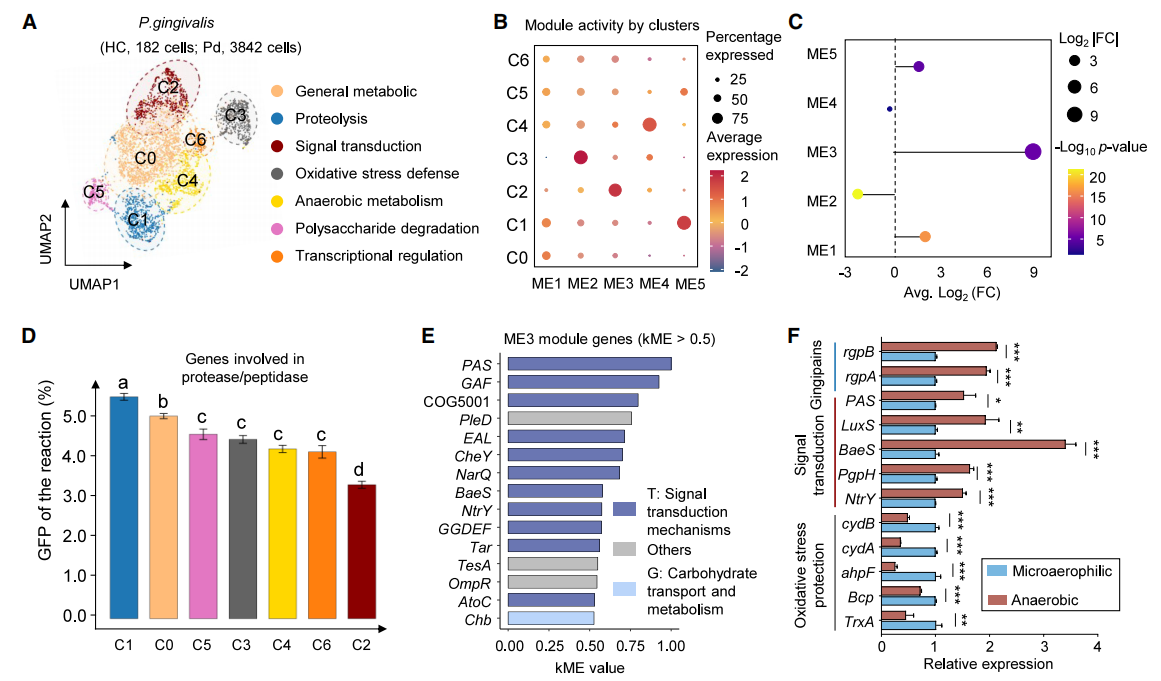
图5. 牙龈卟啉单胞菌转录状态异质性及其在牙周炎中的重塑[4]
综上,VITA OralMicrobiome在口腔菌群研究中展现出重要价值:突破宏组学群体平均限制,可在单个细菌水平解析功能状态与亚群差异,揭示致病菌功能重构与代谢适应。它提供的高分辨率功能信息为理解口腔菌群对健康和疾病的影响,以及制定预防与个体化干预策略提供了关键支撑。
四、VITA OralMicrobiome应用前景
VITA OralMicrobiome 为口腔医学与微生态研究提供了新的高分辨率研究工具:
- 口腔疾病机制研究:深入解析牙周炎等疾病中菌群的功能异质性与代谢重塑。
- 远端器官疾病机制研究:解析口腔菌群的功能状态与代谢活性,阐明其通过血液易位或免疫调节影响阿尔茨海默病、心血管疾病及结直肠癌等远端器官疾病的潜在机制。
- 菌群-宿主互作分析:结合VITA真核单细胞产品,同时分析细菌与口腔上皮/免疫细胞间的分子对话。
- 靶向干预与药物开发:为活菌药物、菌群移植及牙周治疗方案的评价提供高分辨率解析工具。
五、结语
在世界口腔日,我们重新审视这片微小而复杂的生态系统。每一个细菌的转录状态,都是一段关于生存、竞争与致病的微观叙事。长期以来,M20 Genomics专注于新一代单细胞技术的源头创新,持续构建面向复杂微生态样本的检测体系。VITA OralMicrobiome的发布,为全球研究者提供了在单个细菌分辨率下解析口腔菌群功能状态的新工具,为口腔健康及全身健康研究提供了坚实的技术支撑,标志着口腔研究正式告别群体平均,迈入精准特写的新时代。



